深度解讀|2026版《醫療器械生產質量管理規范》新舊對比
核心變化:從10章增至15章,條款從約80條增至132條
2025年11月4日,國家藥監局發布新版《醫療器械生產質量管理規范》(以下簡稱“新版《規范》”),將于2026年11月1日起正式施行。這是自2014年舊版發布以來的一次重大修訂。英碩醫用包裝第一時間組織學習,現將核心變化梳理如下,供行業同仁參考。
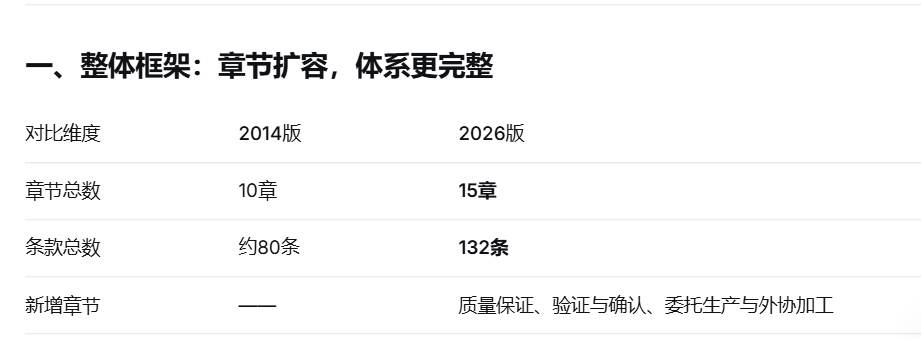
新版《規范》在保留機構與人員、廠房與設施、設備、文件管理、設計開發、采購、生產管理、質量控制、銷售與售后服務、不合格品控制等核心章節的基礎上,新增三個獨立章節,使質量管理體系覆蓋產品全生命周期。
二、三新增章節解讀
1. 質量保證
核心要求:
建立覆蓋產品全生命周期的質量保證體系
規范管理評審與內部審核
將不良事件監測、數據分析、持續改進納入體系閉環
解讀:從“質量控制”向“質量保證”轉變,強調事前預防與持續改進。英碩醫用包裝已建立完善的質量保證體系,并通過ISO 13485:2016認證,為持續合規奠定基礎。
2. 驗證與確認
核心要求:
明確工藝驗證、滅菌驗證、包裝驗證等關鍵環節
強調驗證狀態的持續保持與再驗證
建立驗證主計劃與驗證方案管理
解讀:驗證與確認從“附屬要求”變為“獨立章節”,體現了對過程有效性的高度重視。作為醫用吸塑包裝企業,英碩醫用包裝在密封性能驗證、滅菌適應性驗證等方面持續投入,確保包裝系統符合無菌屏障要求。
3. 委托生產與外協加工
核心要求:
將委托生產、外協加工納入質量管理體系
明確注冊人主體責任與受托方職責劃分
建立供應商動態管理機制
解讀:結合醫療器械注冊人制度,進一步壓實委托生產中的質量責任。英碩醫用包裝作為配套供應商,將持續優化供方管理體系,與客戶共同保障質量安全。
三、重點條款修訂要點
1. 設計開發
主要變化:
風險管理貫穿設計開發全過程
細化設計轉換、設計確認、設計變更要求
強調設計與生產的銜接
2. 采購與物流管理
主要變化:
強化供應商分類管理與動態評價
明確關鍵物料追溯性要求
增加外協加工質量管控
3. 生產管理
主要變化:
細化環境控制與潔凈區管理要求
強化批生產記錄完整性與可追溯性
明確過程控制與工藝參數管理
4. 質量控制
主要變化:
規范放行審核程序與責任
細化檢驗記錄管理要求
強調不合格品控制與糾正預防措施
四、核心導向:三個轉變

五、給行業同仁建議
距離2026年11月1日實施尚有過渡期,建議相關企業:
1. 開展差距分析
對照新版132條要求,逐條評估現有體系的符合性。
2. 完善三大新增板塊
重點關注質量保證、驗證與確認、委托生產三個新增章節的要求落地。
3. 強化關鍵崗位培訓
組織質量負責人、生產負責人、管理者代表等關鍵崗位人員系統學習。
4. 提前自查整改
在過渡期內完成體系優化,確保按時符合新版要求。
結語
新版《規范》的實施,是推動醫療器械產業高質量發展的重要舉措。英碩醫用包裝始終秉持“質量與服務為靈魂”的企業理念,擁有萬級潔凈車間、ISO 13485:2016體系認證,專注于為醫療器械行業提供安全、可靠的吸塑包裝解決方案。我們將持續關注法規動態,與行業同仁一道,共同守護醫療器械質量安全防線。
——責任編輯:英碩包裝
版權所有http://www.beichen531.com轉載請注明出處
相關推薦:
最新產品
同類文章排行
- 重磅解讀 | 醫療器械初包裝微粒污染怎么測?新國標來了!附英碩包裝實戰經驗
- 2026無菌醫療器械常用包裝材料與包裝形式滅菌方式指南
- 深度解讀|2026版《醫療器械生產質量管理規范》新舊對比
- 影響環氧乙烷滅菌效果的因素
- 無菌包裝材料的評估項目及測試方法參考
- 影響醫療器械貨架有效期的因素
- 《醫療器械初包裝的生產環境要求》
- 《最終滅菌醫療器械包裝合規標準參考》
- 疫情期間,醫用吸塑托盤整柜發往國外
- 開發與設計醫療包裝要遵循哪些基本步驟
最新資訊文章
您的瀏覽歷史







 粵ICP備14050553號-1
粵ICP備14050553號-1